电化学势概念简述
电化学势在《电化学原理》一书中又被称为电化学位,对它的定义是一条表达式:
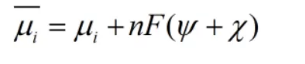
化学位又被成为化学势,是《物理化学》中热力学部分的重要内容之一。它被定义为物质的粒子数量所引起的体系自由能变化,表达式为∂G/∂n(摩尔量所引起的吉布斯自由能变化)。
外电位是电荷所做的一种功。当一个正电荷从无限远处移动至某带电物体外部,并且两者之间可形成长程作用力时,电荷所做的电功。功是能量变化的度量,这里要回顾一下电功和电位的关系。
电荷在电场中会产生势能,而电场中势能与该点处电荷量的比值即为电位。
所以,正电荷所做的功在带电物体外部产生电位,即被称为外电位。
在带电物体外部的正电荷克服短程力进入到物体内部所作的电功即为表面电位。
因此,一个正电荷从无穷远处移动到带电物体内部需要作的电功为外电位与表面电位之和,即ψ+χ。由于这里指的是单个正电荷的情况,所以实际公式中需要再乘以电荷总量,即nF(ψ+χ)。
综上所述,电化学位(电化学势)可被认为是一个正电荷进入带电的电极表面所作的电功与电极自由能改变量之和。
目前,电化学势在理论上主要应用于电解池内物质移动方向判断,也可用于计算电极电势。
小编觉得《物化》教材上的一段话已足够精炼:“正如对于不带电的物体,用化学势可以判断物质自动迁移的方向一样,对于带电的系统,则可用电化学势来判断物质自动迁移的方向”。这里利用读者对化学势的理解代入到电化学势,道理想通,但是小编不同意后半句中说道“可用电化学势来判断物质自动迁移的方向”,由于系统带电,电场产生外部影响,所以这里的迁移不应该自动的,而应是被动的,就像电池充电那样。
那么,利用电化学势的定义式判断带电系统中不同地方电化学势的相对大小就可以知道离子等物质迁移的方向了。而要计算某处电化学势,需要知道某处的电位、化学势(位)以及表面电位等数值。而科学往往条条大道通罗马,若电池为可逆电池,可以利用电势差来间接计算。
电势差=标准电势差+某组分活度对电势改变量,公式如下:
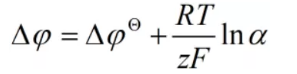
式中φ为电极电势;α为某组分的活度。若为溶液与电极之间的电势差,那么Δφ代表电极电势;若为正负极之间的电势差,那么Δφ可近似代表电池的电动势。
再利用:

就可以得到一系列参数的具体数值。但是这些公式的应用需要诸多条件,如可逆电池、理想溶液(非理想用活度因子)、金属电极等,而实际情况要复杂的多,尤其使用高浓度电解液和、非金属电极、高低温甚至复杂电池构造时,情况都会产生变化。




