金属的各种腐蚀现象及其试验方法
2021-07-09
金属材料全面腐蚀的危害性较局部腐蚀小,也容易防止,而许多零部件是因为局部腐蚀而损坏。1.1 点蚀
点蚀也称孔蚀,是为害最大的腐蚀形式。各种材料都有产生点蚀的可能性,但是不锈钢,铝及其合金,钛及其合金等最易钝化的金属在含有CI- 离子的溶液中最易产生点蚀。发生点蚀的腐蚀介质是含有氧化性金属离子的氯化物(金例如CuCl2, FeCl3等)溶液,而含非氧化性金属离子的氯化物(例如 NaCl, CaCl2等)溶液对点蚀也有影响,但其程度小得多。一般含卤族化合物溶液都可能引起点蚀,其中以 CI-离子最甚,Br-次之,F-、I-离子对点蚀作用较小。1.1.1 化学浸泡法
此法技术成熟,应用广泛,许多国家已有标准。通过测量蚀孔的失重量、数目、尺寸大小及深度,确定材料耐点蚀能力。也可以通过测量临界点蚀温度,蚀孔形核所需最低CI-浓度等,确定材料点蚀敏感性。化学浸泡法常用点蚀试验溶液成分及试验条件如表1 所示。FeCl3溶液中含有大量破坏钝化膜的 CI- 溶液的酸性强,有强烈的点蚀倾向,所以普遍采用 FeCl3 溶液作为点蚀加速试验介质,用以研究材料化学成分、热处理及表面处理与耐点蚀性能关系。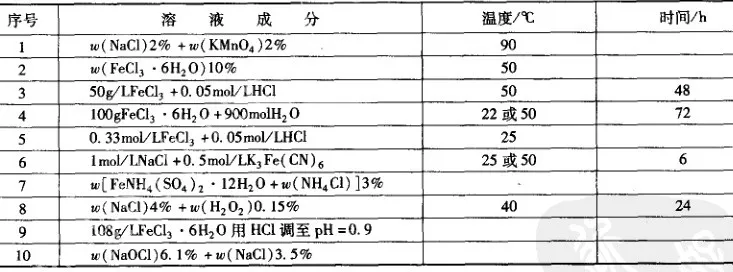
中国、美国及日本曾对不锈钢用FeCl3 溶液进行点蚀试验的主要技术条件如表2 所示,供读者参考。浸泡后的试样用肉眼或放大镜、低倍显微镜进行检查、记录及拍照。然后除掉腐蚀产物,精确称重(0.1mg) , 用带网格的透明纸数出试样单位面积上(1cm²) 蚀孔数目。用蚀孔深度测量仪或光学显微镜测定蚀孔深度。测出20个蚀孔中最大蚀孔深度和10个蚀孔平均深度。
点蚀性能评定时失重法应用最广泛,用点蚀率[g/ (㎡·h) ] 或平均腐蚀速度(mm/a) 表示。图1 所示为美国 ASTM G46-1994点蚀试验标准中,按蚀孔密度、尺寸和深度的评定标准。图1 所示为蚀孔断面特征。
▲图20 点蚀的标准计数图
电化学法有恒电位法、恒电流法及动电位法等,其中以动电位法应用较多,美国、日本等国家已有标准。
电化学法可测量材料的点蚀特征电位(点蚀电位Eb 和保护电位Ep ) , 确定产生点蚀倾向。当金属在介质中的开路电位(或自然腐蚀电位Ep) 大于Ep时、钝化膜开始破裂,开始溶解;如果Ep<E0<Eb 时,表明点蚀未产生。Eb值越大,钝化膜越难破坏,材料抗点蚀性越好。所以通过测定材料的Eb及Ep值可以判断抗点蚀能力。图22所示为用动电位法测量的阳极极化曲线示意图。
在铆接、、螺纹联接的接合部位存在宽度为0.025~0.1mm的缝隙时。易发生缝隙腐蚀。几乎所有腐蚀性介质都能使金属产生缝隙腐蚀,但以含CI-的溶液最易引起这类腐蚀。几乎所有金属都可能发生缝隙腐蚀,但是以钝化型金属最易产生这类腐蚀。
缝隙腐蚀试验与点蚀相似,分为化学浸泡法和电化学法。例如FeCl3 溶液浸泡试验参数与点蚀试验法相同,只是试样尺寸不同,已成为美国缝隙腐蚀试验标准。电化学法用于测定金属的击穿电位和保护电位,测定阳极电流密度等。GB/T10127-2002《不锈钢三氯化铁缝隙腐蚀试验方法》 适用于测定不锈钢及镍铬合金在FeCl3 溶液中的腐蚀速度。
1.3 电偶腐蚀
两个不同腐蚀电位的金属在同一电解液中相接触时,电位低的金属比电位高的腐蚀速度快,例如在室温水中钢与锌成电偶相接触时,锌是阳极产生腐蚀,钢是阴极受到保护。但是水温升至82℃时电偶腐蚀极性逆转,钢变成阳极,锌是阴极,钢遭腐蚀,锌受保护。腐蚀电位是指在该电解液中两种金属各自的实际电位,而非标准电极电位或平衡电位。这种实际电位是各种金属在特定介质中的电位顺序或电偶序。介质性质及极化情况对电偶腐蚀有影响。此外阳极与阴极面积比对电偶腐蚀有影响;大阴极小阳极组成电偶时,阳极腐蚀程度增大。例如Cu 板与钢铆钉和钢板与 Cu 铆钉组成的两种电偶在海水浸泡15个月后,前者钢铆钉腐蚀严重,而后者钢板腐蚀轻微,钢板和铜铆钉连接牢固。电偶腐蚀试验方法有浸泡法和电化学法。
1.3.1 浸泡法
将两种金属按实际面积比例做成电偶试样,捆扎在一起,浸泡在试验介质中。将腐蚀试验结果(用重量法)与未发生电偶腐蚀金属比较。1.3.2 电化学法
电化学法测量电偶腐蚀有三个方面,一是测定电偶电位;二是测定电偶电流;三是测定极化曲线。
1.4 晶间腐蚀
不锈钢、Ni 基合金、AI合金(Al-Cu、Al-Cu-Mg、Al-Zn-Mg及Mg质量分数大于3%的AI-Mg合金)中经常产生晶间腐蚀。晶间腐蚀特点是沿晶界腐蚀,晶粒不腐蚀或腐蚀的很轻微。金属中出现晶间腐蚀后外观无明显变化,但是材料的物理、力学性能几乎全部丧失,造成严重破坏。导致晶间腐蚀的原因有两种理论,一是合金元素贫化,例如奥氏体不锈钢是贫 Cr, Ni-Cr-Mo 合金是贫 Mo, Al-Cu 合金是贫 Cu; 二是选择性溶解,例如奥氏体不锈钢在强氧化性介质中经固溶处理后也产生晶间腐蚀,而经敏化处理后反而不产生晶间腐蚀。这可能是由于固溶处理使P、Si在晶界上偏聚,引起选择性溶解,敏化处理使P、Si 不再富集。晶间腐蚀试验方法很多,其原理及适用范围各不相同,不同的材料和介质应当选用不同方法。晶间腐蚀试验方法可分为三大类,一是化学浸泡法,应用广泛,较为成熟,其中一些方法已被一些国家列为国标;二是电化学法,其特点是试验时间短,不破坏试样;三是物理试验法,其中以金相法和弯曲法应用较广泛。
精川材料检测:http://www.jctest.vip/




