铁质文物的腐蚀机制
01 化学腐蚀
Fe单质铁的还原性并不强,但当有Fe2+存在时,单质Fe会快速从0价态被氧化成高价态。铁器的锈蚀发展是一个连续的过程。Fe首先从0价氧化为+2价,主要反应为析氢腐蚀或者吸氧腐蚀:当铁器在水中浸泡或者表面存在一层酸性水膜,Fe的活泼顺序排在H+之前,会发生置换反应生成Fe2+和H2;当铁器表面直接与空气接触,或与铁器表面接触的水膜呈现中性或碱性,此时Fe与空气或水中溶解的O2发生反应形成Fe2+。形成的Fe2+化合物主要以FeO和Fe(OH)2存在,其会继续与氧化性物质反应生成Fe3O4、Fe2O3和Fe(OH)3等。
以化学腐蚀反应为例,不同环境下铁腐蚀产物的转化反应分类如下所示:
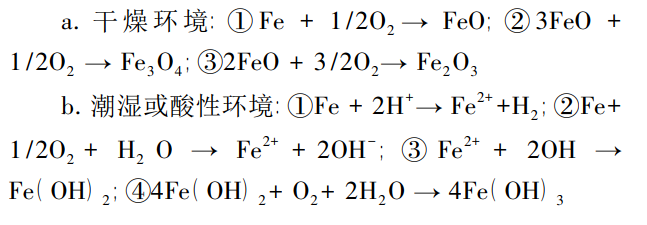
铁器表面的腐蚀产物被分为无害锈和有害锈。无害锈指的是干燥环境下形成的Fe3O4或α-Fe2O3,锈层结构较为致密,覆盖在文物表面可抑制内部的铁进一步腐蚀。有害锈大多是在潮湿环境下形成的FeOOH,根据晶型可将其分为γ-FeOOH、β-FeOOH或α-FeOOH等,结构疏松布满孔隙,外界的腐蚀性介质会通过毛细作用继续渗入。由于有害锈的存在,铁器文物的腐蚀会持续进行,造成严重的矿化、点蚀等病害,必须在修复过程中去除。
在潮湿环境下,外界其他成分如CO2、SO2、NO2、HCl、H2S等还会吸附在铁器表面形成水膜,发生化学腐蚀反应,产生的硫酸铁、碳酸亚铁、氯化铁、硝酸铁等腐蚀产物又会水解形成Fe(OH)3、FeOOH等,加速文物劣化。
另外,部分铁器在冶炼过程中经反复锻打减少了表面微孔,降低了与腐蚀性介质接触面积,耐蚀性相应会提高。但锻打会使得铁器结构分层,是诱发层状或丝状腐蚀等病害的原因之一。
02 电化学腐蚀 通常情况下,电化学腐蚀对铁器文物保护的危害要远远大于化学腐蚀,一旦发生不可控的电化学腐蚀,极易造成文物崩解并损害其考古价值,必须重点关注。 03 腐蚀介质的影响 土壤是由固、气、液组成的多相体系,其中腐蚀反应要比在大气、水中更为复杂。水、可溶盐和氧气会在铁器表面构成电化学腐蚀。在此基础之上,土壤化学组成、氧含量、电阻率、含水率、pH值、微生物种类、杂散电流等理化参数也会参与腐蚀进程,进而生成性质各异的腐蚀产物。这些腐蚀产物与周围土壤混合,覆盖铁质文物表面的考古信息,其中的硬质腐蚀产物会形成硬结物覆盖表面,造成硬结物病害。铁器文物大多数是从墓葬环境中发掘,土壤腐蚀在所有腐蚀介质中最具代表性。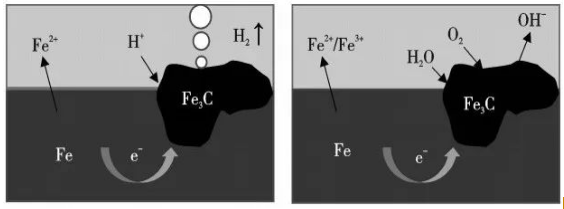 图1 铁器表面的微电池腐蚀反应
图1 铁器表面的微电池腐蚀反应




